Биологи впервые отследили процесс проникновения ВИЧ в клетки человека
-
Американские ученые впервые смогли детально проследить, как ВИЧ проникает в клетки человека и вставляет свой геном в их ДНК. Оказалось, что значимую роль в этом процессе играет оболочка вируса. Например, если она разрушается, размножение вируса прекращается.
Подробнее:
-
Участник @васьвась написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
Оказалось, что значимую роль в этом процессе играет оболочка вируса.
Да ну, не может быть! =) А я-то думал, что оболочка вируса - совершенно рудимент этого самого вируса и не играет никакой роли. А в клетку он проникает по флаерам, или потому что у него батя - CD4.
-
Участник @april написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
считалось, что оболочка несёт только защитную функцию для содержимого капсида
Хз кем это считалось. Это вроде базовые вещи биологии. Еще в школе проходили. В клетку что попало проникнуть не может, для этого у вирусов есть на поверхности какие-то лиганды, благодаря которым они в клетку проникают.
Участник @april написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
Как минимум, могут появится новые классы АРВТ
Более прущие, с фрактальчиками =)
-
Участник @april написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
Как минимум, могут появится новые классы АРВТ
Гилхед выкатывал уже вроде ингибитор капсида года 3 назад
-
Вообще, в свете данного и, например, вот этого недавнего исследования, кроме отрицательного для нас момента, заключающегося в том, что капсид-злодей успешно играет важную роль «защитника» (от клеточных факторов хозяина в цитоплазме) и «защитника-участника» процессов обратной транскрипции и интеграции, соответственно, можно выделить и положительный для нас момент.
Он вытекает из отрицательного момента и заключается в следующем:
при одновременной атаке клетки-мишени несколькими образовавшимися из разных провирусных ДНК, генетически разнообразными вирионами (в том числе, разнообразными монолекарственно устойчивыми мутантами), вследствие того, что капсид вириона полностью распадается лишь в ядре клетки – в цитоплазме не происходит:
а) обмена между разновирионными геномными РНК и разновирионными ревертазами (в том числе при рекомбинациях) во время обратных транскрипций;
б) обмена между образовавшимися разнородными вирусными ДНК и разновирионными интегразами во время образования прединтеграционных комплексов.Т.е. данная особенность поведения капсида ВИЧ значительно понижает:
1) генетическое разнообразие вируса;
2) шансы на образование мультирезистентных штаммов вируса;
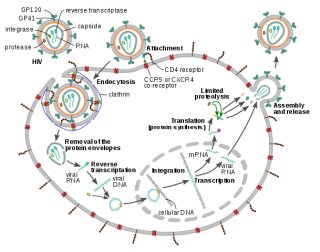
3) шансы на обход комбинированных схем АРВТ с НИОТами, ННИОТами и ИИ в составе.P.S. Кстати, по старинке в подавляющем большинстве изображений в интернете жизненный цикл ВИЧ иллюстрируется с «раздеванием» капсида в цитоплазме клетки, что в свете современных сведений уже не совсем корректно. Вот, например, ниже картинка из Wikipedia:
-
А как из ядра удаляются гм… “ошметки” вирусного капсида?
И почему а) и б) не может происходить внутри ядра, например? Там же тоже жижка, кареоплазма, или как ее там
-
Участник @just_one написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
И почему а) и б) не может происходить внутри ядра, например? Там же тоже жижка, кареоплазма, или как ее там
а) не может, т.к. строительный материал для обр.тр-ции- нуклеотидтрифосфаты находятся только в цитоплазме и потому что капсид разрушается окончательно только после завершения обратной транскрипции как раз. За счёт выпучивания двухспиральной ДНК как раз капсид и рвётся, т.е. в ядре клетки уже нет РНК, она разрушена РНКазной активностью ревертазы внутри капсида ещё.
б) не может, т.к. прочный прединтеграционный комплекс из тетрамера интеграз и вирусной ДНК (интасома ВИЧ) и клеточных факторов уже сформирован внутри капсида (за счёт межмолекулярных взаимодействий близко находящихся друг от друга внутри капсида интеграз и концов вирусной ДНК) и смысла внутри ядра клетки с энергетической точки зрения для комплексов/интасом распадаться и обмениваться интегразами - уже нет, они уже готовый к интеграции прочный продукт.
Плюс, многие вспомогательные клеточные факторы хозяина присутствуют в цитоплазме (например, необходимый для образования прединтеграционного комплекса протеин LEDGF/p75).
-
@gremlin ух е, через слово понятно только. Но общий смысл уловил, спасибо. Так а куда белки из ядра деваются от распавшегося капсида? Я так понимаю, через мембрану ядра не каждая молекула пролезет.
-
Участник @just_one написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
Так а куда белки из ядра деваются от распавшегося капсида?
А вот насчёт этого, честно говоря, не задумывался)). А из школьной биологии уже не помню. Наверняка какой-то механизм предусмотрен для этого. Надо глянуть будет в инете.
-
Участник @just_one написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
через слово понятно только
Такая же уйня)
-
Участник @just_one написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
Так а куда белки из ядра деваются от распавшегося капсида? Я так понимаю, через мембрану ядра не каждая молекула пролезет.
Загуглил слегка. Я так понял, в ядре есть некие экспортные сигнальные белки, которые после того как капсид ВИЧ распался, способствуют выводу из ядра через ядерные поры структурных компонентов капсида - пентамеров р24, возможно, за счёт активного транспорта (если эти пентамеры недостаточно малы для пассивного транспорта), а уже затем в цитоплазме метятся убиквитином и разрезаются в протеасоме клеточными протеазами до цепочек из нескольких аминокислот. А вот импорт не совсем маленького капсида ВИЧ в ядро, похоже, по-любому осуществляется за счёт активного (с затратами энергии) транспорта через поры ядра с привлечением клеточных факторов хозяина.
-
Участник @васьвась написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
Участник @just_one написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
через слово понятно только
Такая же уйня)
Надо просто постараться детально с иллюстрациями максимально подробно описать механизмы обратной транскрипции и интеграции ВИЧ и тогда все сложится по полочкам само.
-
Участник @gremlin написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
а) обмена между разновирионными геномными РНК и разновирионными ревертазами (в том числе при рекомбинациях) во время обратных транскрипций;
Ретровирь псевдодиплоидный – два полных генома в РНК несет, но эти два полных генома транслируются в одну провирусную ДНК, и вот тут и происходит рекомбинация (два сценария, см. PMID: 30307534, и с гомозиготами просто тут результат не отследить никак. Интересно, считал ли кто сколько тех самых гомозигот… к чему я. А так ли важно, если у тебя две РНК, меняться промеж вирусов? Разнообразие и в двух соседних РНК будет, если будет, то же (не принципиально иным), на первый взгляд, как и с РНК из другого вириона. Нет? Не уверен тут.
-
Участник @gremlin написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
через поры ядра
Коразтыкенет. Не через поры. В том и фишка этого ядерного эндоцитоза, поры по боку.
It was found that after entering the cell, the viral particles moved along the microtubules and selectively gathered at the microtubule organization center (MTOC), leading the nearby nuclear envelope (NE) to undergo deformation, invagination and restoration to form a nuclear vesicle in which the viral particles were wrapped; then, the inner membrane of the nuclear vesicle ruptured to release HIV-1 into the nucleus. This phenomenon is similar to cell endocytosis and therefore called the “nuclear endocytosis-like pathway”. Factors involving in the process were preliminarily investigated. This discovery expands our understanding of the complexity of HIV-1 nuclear entry, which may provide new insights to HIV-1 virology. The molecular details and viral biology of the mechanism need further elucidation.
-
Участник @ilya-antipin написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
А так ли важно, если у тебя две РНК, меняться промеж вирусов? Разнообразие и в двух соседних РНК будет, если будет, то же (не принципиально иным), на первый взгляд, как и с РНК из другого вириона. Нет? Не уверен тут.
Однозначно, считаю, что разнообразие было бы намного выше при существовании такого «разновирионнорекомбинантного» механизма. И намного опасней с точки зрения возникновения лекарственно-устойчивых штаммов.
Гетерозиготы ВИЧ могут появляться только при условии наличия сразу не менее 2-х разных провирусных ДНК в геноме инфицированной клетки. Причем выход гетерозигот при, например, 2-х провирусных ДНК в среднем будет около 50% в сравнении с гомозиготами.
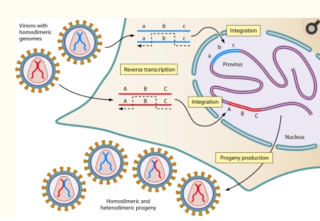
А вот таких клеток (с 2-мя и более провирусами в геноме) в организме, что недавно инфицированных, что хронически инфицированных пациентов не более 10, максимум 15% [1], [2], [3].
Предположим, у нас есть 10 клеток с разными провирусными ДНК в составе. Пусть согласно исследованиям 9 клеток несут один провирус, а 1 клетка несет 2 провируса в геноме. Пусть все эти 11 провирусных ДНК имеют каждая по одной какой-либо разной мутации устойчивости, в том числе к разным классам препаратов.
Тогда при их реактивации в более-менее один временной период эта армада, состоящая из приблизительно 19/20 части гомозиготных и 1/20 части (50% от 1/10) гетерозиготных вирионов рассеется по организму и клеткам. И уже на этой стадии, т.к. разные вирионы, по-любому, будут залетать в одни и те же клетки, в случае возможности «межвирионной» рекомбинации в цитоплазме начнут со страшной силой смешиваться и образовывать всевозможные мутанты (ревертаза прыгает с шаблона на шаблон РНК от 5 до 10 раз), в том числе мультирезистентные. И тем более, вичевые ревертазы не будут ограничиваться скачками только «туда-обратно» меж 2-х РНК, а будут скакать, как угорелые, между множеством шаблонов вирусных РНК «туда-сюда-туды-сюды-обратно», типа того. Т.е., практически, каждая вновь инфицированная клетка будет обладать би-, либо полимутантными провирусными ДНК.
А вот, если ревертазе ВИЧ можно скакать только внутри капсида, то потенциальный (но еще не готовый) рекомбинант сможет образоваться только из 10% вновь инфицированных клеток, где будет «впаяно» по 2 и более провируса на клеточную ДНК. И то рекомбинант от этих клеток будет образовываться где-то в 50% дочерней популяции и к тому же будет содержать одновременно лишь не более 2-х мутаций устойчивости (т.к. РНК смешиваться в один вирион будут только по 2-е, хоть из 2-х, хоть из 5-и одновременно «впаяных» в геном клетки разных провирусов), максимум 3-х мутаций устойчивости (в случае, если один из провирусов в геноме клетки происходит от атаки 1/20 гетерозиготной части вирионов).
И так далее по циклу преимущество в диверсификации «межвирионнорекомбинантной» популяции по сравнению с «внутрикапсиднорекомбинантной» популяцией будет только наращиваться.Оно и понятно, если бы такая «межвирионная» рекомбинация была возможна, то мы бы имели на сегодня кучу полирезистентных штаммов ВИЧ у каждого пациента.
Но конечно, технически, наверняка, было бы сложно ревертазам в цитоплазме на расстояниях скакать с РНК на РНК, нежели компактно внутри капсида. Но это уже другой вопрос
-
Участник @ilya-antipin написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
Коразтыкенет. Не через поры. В том и фишка этого ядерного эндоцитоза, поры по боку.
Да, конечно, там же все черным по белому было написано.
“nuclear endocytosis-like pathway”
Бес дернул меня наускоре накинуть про импорт в ядро.))
А по поводу экспорта из ядра, как думаете?
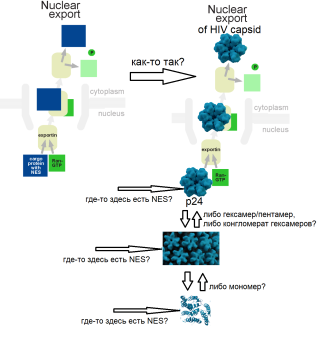
У меня такая версия: я так, подозреваю, что на гекса(пента)мере капсида p24 где-то есть аминокислотная метка (ядерный экспортный сигнал NES) для экспортина и Ran-GTP. Подозреваю, что эта «метка» замаскирована, когда капсид в сборе, а вот когда разбирается, то она оголяется. Вот только до каких структурных элементов разбирается капсид? До мономеров, до гексамеров, или до конгломератов гексамеров? И, следовательно, при разборке капсида до какого структурного элемента, метка (NES) оголяется и становится видимой для экспортин- Ran-GTP комплекса?
Типа того:
??? -
Участник @gremlin написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
про импорт в ядро.))
А по поводу экспорта из ядра, как думаете?Может я ошибаюсь, но нужны секторальные санкции на импорт. И чтобы запрещенка не проникла даже через Беларусь. А если проникнет, то давить ее бульдозером .
-
Участник @gremlin написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
Гетерозиготы ВИЧ могут появляться только при условии наличия сразу не менее 2-х разных провирусных ДНК в геноме инфицированной клетки.
А точность обратной транскриптазы мы здесь игнорируем? Сколько там… 5-10 на 9000 помню, 1/1700 замен/добавлений/делеций помню цифру… Ну, или тут почитать можно.
-
@васьвась а лучше давить тракторами не запрещенку, а тех, кто ее ел.
-
Участник @gremlin написал в Биологи впервые отследили процесс проникновения ВИЧ в клетки человека:
А по поводу экспорта из ядра, как думаете?
Стараюсь не думать об этом )) Я в такого рода вопросах все же склонен ждать, когда большие пацаны определятся, все разжуют для моего уровня, и вот тогда кушать уже и других кормить.